дкбаОПШШСІбЇЮЪЬтЪБЃЌашЪзЯШШЗЖЈбаОПЕФЖдЯѓЃЌМДЫљЮНЬхЯЕЁЃЬхЯЕЕФЭтНчГЦЮЊЛЗОГЁЃЬхЯЕЕФШЗЖЈЪЧИљОнбаОПЕФашвЊШЫЮЊЛЎЗжЕФЁЃЮЊСЫбаОПЗНБуЃЌЭЈГЃАбЛЏбЇЗДгІжаЫљгаЕФЗДгІЮяКЭЩњГЩЮяЕБзїЮЊЬхЯЕЁЃЕБзХблгкЬхЯЕгыЛЗОГжЎМфЕФФмСПКЭЮяжЪЕФНЛЛЛЧщПіЪБЃЌПЩНЋЬхЯЕЗжГЩШ§жжЃКгыЛЗОГжЎМфМШгаЮяжЪНЛЛЛгжгаФмСПНЛЛЛЕФЬхЯЕНаГЈПЊЬхЯЕЃЛгыЛЗОГжЎМфЮоЮяжЪНЛЛЛЖјгаФмСПНЛЛЛЕФЬхЯЕНаЗтБеЬхЯЕЃЛгыЛЗОГжЎМфМШЮоЮяжЪНЛЛЛгжЮоФмСПНЛЛЛЕФЬхЯЕНаЙТСЂЬхЯЕЁЃгЩгкЭЈГЃАбЗДгІжаЫљгаЗДгІЮяКЭЩњГЩЮябЁзїЮЊЬхЯЕЃЌвђДЫЛЏбЇЗДгІЪЧЗтБеЬхЯЕЁЃЬхЯЕгыЛЗОГжЎМфПЩвдгаФмСПНЛЛЛвВПЩвдУЛгаФмСПНЛЛЛЃЌЕЋЪЧЃЌДѓСПЕФЪТЪЕЫЕУїгюжцМфЕФзмФмСПЪЧЪиКуЕФЃЌМДФмСПМШВЛДДЩњвВВЛФмЯћУ№ЃЌетОЭЪЧФмСПЪиКуЖЈТЩЁЃ
ЖдгквЛИіЗтБеЬхЯЕЃЌЬхЯЕЕФШШСІбЇФмЮЊU1ЃЌЬхЯЕДгЛЗОГЮќЪеСЫШШСПQЃЌЭЌЪБЬхЯЕгжЖдЛЗОГзіЙІWЃЌетЪБЬхЯЕЕФШШСІбЇФмБфЮЊU2ЁЃИљОнФмСПЪиКуЕУЕН
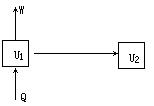
U1 Q-W=U2
U2-U1=Q-W
МД ΔU= Q-W
етОЭЪЧШШСІбЇЕквЛЖЈТЩЁЃвђДЫЃЌШШСІбЇЕквЛЖЈТЩОЭЪЧФмСПЪиКуЖЈТЩдкШШСІбЇЩЯЕФОпЬхЬхЯжЁЃЮвУЧЙцЖЈЬхЯЕЮќЪеШШСПQЮЊе§жЕЃЌЬхЯЕЗХГіШШСПQЮЊИКжЕЃЛЬхЯЕЖдЛЗОГзіЙІWЮЊе§жЕЃЌЛЗОГЖдЬхЯЕзіЙІWЮЊИКжЕЁЃЬхЯЕШШСІбЇФмдіМгΔUЮЊе§жЕЃЌЬхЯЕШШСІбЇФмМѕЩйΔUЮЊИКжЕЁЃ
ЬхЯЕШШСІбЇФмUЪЧзДЬЌКЏЪ§ЁЃОЭЪЧЫЕЃЌЬхЯЕЕФзДЬЌШЗЖЈСЫЃЌЬхЯЕЕФШШСІбЇФмвВОЭШЗЖЈСЫЁЃМДЬхЯЕШШСІбЇФмБфЛЏ(ΔU)жЛШЁОігкЬхЯЕЕФжеСЫзДЬЌгыЦ№ЪМзДЬЌЃЌгыЬхЯЕДгЪМЬЌБфЕНжеЬЌЕФРњГЬЮоЙиЁЃ
ЙІКЭШШЪЧЗЧзДЬЌКЏЪ§ЁЃЮвУЧВЛФмЫЕЬхЯЕОпгаЖрЩйЙІЛђЖрЩйШШЃЌжЛФмЫЕЬхЯЕгыЛЗОГНЛЛЛСЫЖрЩйЙІКЭШШЁЃНЛЛЛЕФЙІКЭШШЕФДѓаЁВЛНігыЬхЯЕЕФЪМФЉзДЬЌгаЙиЃЌЛЙгыЬхЯЕДгЪМЬЌБфЛЏЕНжеЬЌЕФРњГЬгаЙиЁЃЫљвдЙІКЭШШвВНаЙ§ГЬКЏЪ§ЁЃ




